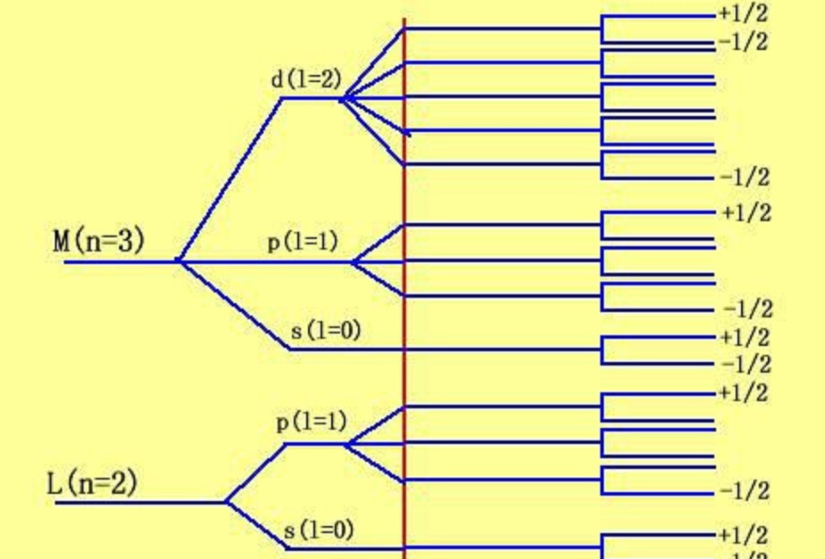
磷的四个量子数是什么 四个量子数怎么求出来的
四个量子数指的是什么?量子力学里的4个量子数 n l m ms 具体物理意义是什么?一至二十号元素所对应的四个量子数,四个量子数分别是,四个量子数是什么?四个量子数是指什么?
本文导航
四个量子数怎么求出来的
n、l、ml、ms
主量子数,角量子数,磁量子数,自旋量子数
主量子数和次量子数的关系
主量子数:量子能级,方位角量子数:量子角动量,磁量子数:量子磁矩,自旋量子数:量子自旋量子数。
主量子数是量子能级量子化的结果,这个百度上有,方位角量子数是波尔在推倒量子能级方程时提出的,是量子的位置矢量和角动量的矢量积,磁量子数百度上有;
自旋是假设量子可绕自身轴线旋转,这会产生一个局部磁场,而这个磁场可能有两个方向,从而形成两个不同的能态,电子的自旋态可有狄拉克电子相对论方程得出。
扩展资料:
量子数表征原子、分子、原子核或亚原子粒子状态和性质的数。通常取整数或半整数分立值。量子数是这些粒子系统内部一定相互作用下存在某些守恒量的反映,与这些守恒量相联系的量子数又称为好量子数,它们可表征粒子系统的状态和性质。
在原子物理学中,对于单电子原子(包括碱金属原子)处于一定的状态,有一定的能量、轨道角动量、自旋角动量和总角动量。表征其性质的量子数是主量子数n、角量子数l、自旋量子数ms=1/2,和总角动量量子数j。
四个量子数咋算
主量子数n:前20号元素的主量子数为1,2,3,4,5,6【摘要】
一至二十号元素所对应的四个量子数【提问】
主量子数n:前20号元素的主量子数为1,2,3,4,5,6【回答】
1至20号元素所对应的电子的四个量子数
【提问】
角量子数位主量子数减一【回答】
自旋量子数的取值为±1/2【回答】
我的意思是你把1至20号元素所对应的电子的四个量子数分别写出来发给我呢【提问】
磁量子数为±角量子数【回答】
这个没有【回答】
那你随便挑一个元素举个例子总行吧,这我啥也没懂呀,【提问】
第一个元素,氢,电子层数为1,所以主量子数为1,然后角量子数是主量子数减1等于0,自旋量子数的取值只有±1/2两种,磁量子数的取值数为由角量子数取值决定,氢的等于±1【回答】
1.主量子数n 描述原子中电子出现几率最大区域离核的远近(电子层数); 决定电子能量高低。 取值: n=1 2 3 4 5 6 …… 电子层符号 K L M N O P…… 对于氢原子其能量高低取决于n 但对于多电子原子,电子的能量除受电子层影响,还因原子轨道形状不同而异,(即受角量子数影响) (2) 角量子数l,它决定了原子轨道或电子云的形状或表示电子亚层(同一n层中不同分层) 意义: 在多电子原子中,角量子数与主量子数一起决定电子的能量。 之所以称l为角量子数,是因为它与电子运动的角动量M有关。 如 M=0时,说明原子中电子运动情况同角度无关,即原子轨道或电子云形状是球形对称的。 .角量子数,l只能取一定数值 l = 0 1 2 3 4 ……(n-1) 电子亚层 s p d f g 说明M是量子化的,具体物理意义是:电子云(或原子轨道)有几种固定形状,不是任意的。 如: s p d f 球形对称 哑铃形 花瓣形 180,90棒锤形 第一电子层 仅有 l s 电子,(l =0) 第二电子层 有 2s,2p电子(l =0, 1) 第三电子层 有 3s, 3p, 3d 电子 (l =0, 1, 2…) 依此类推。见p76表3-2 .对H和类氢离子来说: E1s<E2s<E3s<E4s E4s=E4p=E4d=E4f 但对多电子原子来说:存在着电子之间的相互作用,n相同,l不同时,其能量也不相等【回答】
氢核外只有一个电子,那核外有很多的呢,比如P元素呢【提问】
知道电子层数吧【回答】
n=1 2 3 4 5 6 …… 电子层符号 K L M N O P…【回答】
主量子数就是它的电子层数【回答】
以氧元素为例:氧原子中的所有8个电子的4个量子数,每1横行表示1个电子。按电子所在轨道离原子核距离由近到远,从上到下依次排列(在能量相同的轨道上,电子排列就不分先后了):
主量子数,角量子数,磁量子数,自旋数(m后面的s是下标字母)
n=1,l=0,m=0,ms=+1/2
n=1,l=0,m=0,ms=-1/2
n=2,l=0,m=0,ms=+1/2
n=2,l=0,m=0,ms=-1/2
n=2,l=1,m=+1,ms=+1/2
n=2,l=1,m=+1,ms=-1/2
n=2,l=1,m=0,ms=+1/2
n=2,l=1,m=-1,ms=+1/2【回答】
自旋量子数什么时候是正的二分之一什么时候是负的,这些正负号怎么判断的【提问】
自旋本质上没有正负的区分,只有方向不同的区分。
我们所谓的自旋正负,是一种人为的规定。比如,我们规定向左的自旋为正,向右的自旋为负。这种正负的区分,不具有物理本质。我们也可以规定向右的自旋为正,向左的自旋为负。【回答】
规定一个正负,只是为了数学表达的需要,不具有物理本质。这是一种物理学通用的表示方法。如果连这个都不能理解,很难正确理解物理学的实质。【回答】
四个量子数的意义和取值要求
主量子数(n),角量子数(l;),磁量子数(m),自旋量子数(ms)。四个量子数在量子力学中用来描述原子内核外电子运动的状态。主量子数是描述核外电子距离核的远近,主量子数决定了原子轨道能级的高低,n越大,电子的能级越大。n是决定电子能量主要量子数。
量子数介绍
在同一电子层内,电子的能量也有所差别,运动状态也有所不同,即一个电子层还可分为若干个能量稍有差别、原子轨道形状不同的亚层。l的数值不同,原子轨道或电子云的形状就不同,l的取值受n的限制,可以取从0到n减1的正整数。
原子轨道不仅有一定的形状,并且还具有不同的空间伸展方向。磁量子数m(就是用来描述原子轨道在空间的伸展方向的)。通常把n、l、m都确定的电子运动状态称原子轨道,因此s亚层只有一个原子轨道,p亚层有3个原子轨道,d亚层有5个原子轨道,f亚层有7个原子轨道。
简要说明四个量子数的物理意义
1、主量子数:
当主量子数增加时,原子轨道变大,原子的外层电子将处于更高的能量值(能量值只能取确定的、分离的值,这些能量值称为能级),因此受到原子核的束缚更小。这是波尔模型引入的唯一一个量子数。
主量子数n是用来描述原子中电子出现几率最大区域离核的远近,或者说它是决定电子层组数的。因为电子排布遵循最低能量原理排布顺序为ns→(n-2)f→(n-1)d→np,故当主量子数等于3时能级排到1s2s2p3s3p4s3d。
2、角量子数:
角量子数l确定原子轨道的形状并在多电子原子中和主量子数一起决定电子的能级。电子绕核运动,不仅具有一定的能量,而且也有一定的角动量M, 它的大小同原子轨道的形状有密切关系。例如M=0时,即l=0时说明原子中电子运动情况同角度无关,即原子轨道的轨道是球形对称的;如l=1时,其原子轨道呈哑铃形分布;如l=2时,则呈花瓣形分布。
3、磁量子数:
磁量子数代表每个亚层的轨道(轨道方向)。同一亚层(l值相同)的几条轨道对原子核的取向不同。为了解释磁场对原子光谱的影响,量子理论必须进一步予以扩充。
按照经典理论,电子在磁场中的能量取决于和轨道运动及自旋运动:有关的磁矩的取向,因而正是磁场使得某一给定的能级扩展为与电子在磁场中的磁矩的平行和反平行相对应的两个能量值之间的很狭窄的能量范围。
4、自旋量子数:
自旋量子数用ms表示,是描述轨道电子特征的量子数。对于像光子、电子、各种夸克这样的基本粒子,理论和实验研究都已经发现它们所具有的自旋无法解释为它们所包含的更小单元围绕质心的自转(参见经典电子半径)。由于这些不可再分的基本粒子可以认为是真正的点粒子,因此自旋与质量、电量一样,是基本粒子的内禀性质。
自旋与统计:
粒子的自旋对于其在统计力学中的性质具有深刻的影响,具有半整数自旋的粒子遵循费米-狄拉克统计,称为费米子,它们必须占据反对称的量子态(参阅可区分粒子),这种性质要求费米子不能占据相同的量子态,这被称为泡利不相容原理。
另一方面,具有整数自旋的粒子遵循玻色-爱因斯坦统计,称为玻色子,这些粒子可以占据对称的量子态,因此可以占据相同的量子态。对此的证明称为自旋统计理论,依据的是量子力学以及狭义相对论。事实上,自旋与统计的联系是狭义相对论的一个重要结论。
四个量子数对应关系表格
四个量子数是指决定轨道或电子能量主量子数。决定电子空间运动的角动量角量子数,决定原子轨道的伸展方向磁量子数,描述轨道电子特征自旋量子数。
四个量子数定义
量子数表征原子、分子、原子核或亚原子粒子状态和性质的数。通常取整数或半整数分立值。量子数是这些粒子系统内部一定相互作用下存在某些守恒量的反映,与这些守恒量相联系的量子数又称为好量子数,它们可表征粒子系统的状态和性质。
在原子物理学中,对于单电子原子包括碱金属原子处于一定的状态,有一定的能量、轨道角动量、自旋角动量和总角动量。表征其性质的量子数是主量子数n、角量子数l、自旋量子数ms等于12,和总角动量量子数j。