化学势和溶解度什么关系 判断物质溶解性的方法
物质溶解度由什么决定?物质的溶解性取决于什么?如何知道一种溶质在溶剂中的溶解度?什么什么本身的性质同一温度下溶质溶剂不同溶解度不同?饱和溶液中溶质的化学势与纯溶质的化学势的关系式,饱和溶液中溶剂的化学式u与纯溶剂的化学式u*的关系式。
本文导航
一种物质的溶解度受什么的影响
化学势,我个人是理解为当一种物质溶解到另种物质中时所产生的能量变化吧,我也没学过。
溶解度的大小与许多因素都有关,比如说原子或者分子的结构不同,就决定着他的溶解度是多少。还有比如温度,溶剂的种类,压强(多指气体)。
至于你说的铁等金属和大多气体都很难溶于水我像是因为它们的原子或分子结构很稳定吧。而NaCl易溶于水是因为它是由Na+和Cl-由于离子键而构成的,离子键就是阴阳离子间的一种相互作用。当他放到水里后,水分子会破坏它们之间的离子键,从而变为了游离的Na+和Cl-两种离子存在于水中。
判断物质溶解性的方法
即分子结构相似的物质都是易于互相溶解的,物质的溶解性可以根据在溶剂手册等工具书中查到溶解度数据加以判断。按照物理化学,溶解性质则由溶解的化学势变化来衡量,并用溶解度参数进行定量。在此理论中,物质聚集状态和物理性质取决于分子的几何排列方式和非键合的原子间作用力,这种作用力包括范德华力(色散力,诱导力,偶极矩)和氢键,其强度特征通常由Hildebran提出的溶解度参数表征,溶解度参数因此也由色散组分、极性组分和氢键组分构成,根据它的大小可以进行多组分体系相平衡计算、乳化体系的稳定性研究、高聚物增塑体系的研究及增塑剂的选择、高聚物溶解性预测与研究、高聚物共混物的增溶剂研究、涂料溶剂的选择、油田化学品溶解性研究、溶剂萃取、气体在液体中的溶解研究及膜渗透考察等。溶剂对溶质的分子作用力强的更易于溶解,比如硫酸钡在水中溶解度小的原因在于水分子对硫酸钡的分子作用力小于聚集态硫酸钡分子间的力,硫酸钡溶解的化学势变化为正,因而溶解很难进行。溶剂的溶解度参数可以在相关文献中查到,也可以通过蒸发热数据实验测定或通过基团贡献计算模拟得到。
如何判断溶质和溶剂
从理论上说,是化学势的不同造成了溶质的迁移。
简单地说,就是因为溶解度高(准确的说是溶解能力强)的溶剂与溶质具有更强的亲和力,比如氯化钠与水分子的亲和力(离子化,水合)显然要强于氯化钠和汽油。因此水相部分会把溶质给拽过去,这就是你说的扩散了。类似的,脂肪与汽油的亲和力(分子间作用力)要强于它和水,所以脂肪会向汽油中迁移。碘的萃取也是这样的机理。
溶解度的大小和溶剂的质量有关吗
化学势
溶质在溶液里的化学势和在固体里的化学势相等时,溶解就达到平衡,就是饱和了…
溶质与溶液浓度的关系公式
相等!不用算的,因为饱和溶液中达动态平衡,相平衡的条件就是化学势相等……如果是过饱和的!就是它大于纯溶质的化学势了!
溶液和溶剂的判别方法
饱和溶液中溶剂的化学式u与纯溶剂的化学式u*的关系式:w=S/(S+100),其中w表示饱和溶液中溶质的质量分数,S表示溶解度。
饱和溶液中物质的化学势大于纯溶质化学势,而在不饱和溶液中纯物质化学势大于溶液物质的化学势。一定温度、压力下,当溶液中溶质的浓度已超过该温度、压力下溶质的溶解度,而溶质仍不析出的现象叫过饱和现象,此时的溶液称为过饱和溶液。
溶解度
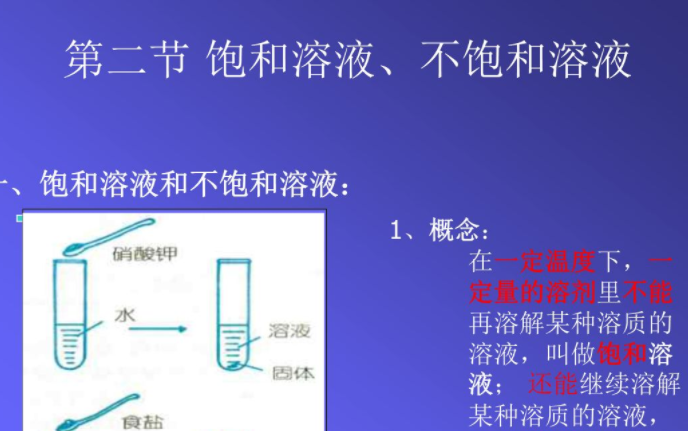
例如在室温下,20mL水中所能溶解的氯化钠的质量有一个最大值,这个最大质量就是形成它的饱和溶液时所能溶解的质量。这说明在一定温度下,在一定量溶剂里溶质的溶解量是有一定限度的。化学上用溶解度表示这种溶解的限度。
溶解度是指在一定温度和压力下一定量饱和溶液中溶质的含量。习惯上把100g溶剂中达到饱和状态时所溶解的溶质的质量叫做这种溶质在这种溶剂中的溶解度。如果没有指明溶剂,则通常所说的溶解度是指物质在水里的溶解度。
以上内容参考:百度百科-饱和溶液